Um eine Antwort auf die Frage zu finden, wie wir die Zahl der erfolgreichen IVF noch steigern können, müssen wir zunächst verstehen, aus welchen Gründen IVF scheitern.
Unsere Patientinnen haben oft mehr als einen Grund, warum sie noch nicht schwanger geworden sind oder warum sich die Schwangerschaften nicht bis zur vollen Dauer entwickelt haben. Andernfalls hätten die ersten IVF-Versuche in ihren örtlichen Kliniken bereits zu einem Ergebnis geführt, und wir hätten uns nie getroffen.
Um jeden Grund für das Scheitern einer IVF zu beseitigen oder zu korrigieren, halten wir uns an das Prinzip „Für jede Herausforderung gibt es eine Lösung".
Dieser Ansatz ist nicht neu: Wenn man ein großes Projekt hat, neigt man dazu, es in mehrere kleinere Projekte mit kleineren Zielen aufzuteilen, die zu einem großen Ziel führen. Die kleineren Ziele sind hier: die Eizellen, die Blastozysten, die chromosomal normalen Blastozysten, die vorbereitete Gebärmutter, das fertige Implantationsfenster und schließlich eine chromosomal normale Blastozyste in die fertige Gebärmutterschleimhaut zum richtigen Zeitpunkt einzusetzen.
Das einzige große Ziel ist ein Baby
Die Gründe für das Scheitern der IVF und den Schwangerschaftsverlust lassen sich in zwei Gruppen einteilen: embryonale und mütterliche Ursachen.
Embryonale Ursachen für IVF-Versagen und Schwangerschaftsverlust bedeuten, dass es im Inneren des Embryos einen Defekt gibt, der ihn nicht lebens- und entwicklungsfähig macht, selbst unter den besten mütterlichen Bedingungen.
Mütterliche Ursachen für das Scheitern der IVF und den Schwangerschaftsverlust umfassen Ursachen innerhalb des weiblichen Organismus und können durch hormonelle, immunologische oder uterine Faktoren erklärt werden.
Überwindung der embryonalen Ursachen für Schwangerschaftsverlust und IVF-Versagen
Embryonale Gründe für den Schwangerschaftsverlust und das Scheitern der IVF sind am stärksten und zu mindestens 75 % für das Ergebnis der Fruchtbarkeitsbehandlung und die Schwangerschaft verantwortlich.
Abbildung 1. Wer ist für das Resultat der IVF-Behandlung verantwortlich – die Frau oder der Embryo?
1. Genetische Situation bei menschlichen Embryonen

- Menschliche Embryonen von Frauen nach dem 35. Lebensjahr haben oft einen abnormalen Chromosomensatz [Fragouli et al., 2012], und das ist, so seltsam es klingen mag, normal.
- Ein abnormaler Chromosomensatz im Embryo führt fast immer zu einem Schwangerschaftsverlust in der Präimplantationsphase (Implantationsversagen) oder in der Postimplantationsphase (Fehlgeburt) [Scott at al., 2012].
- Ein abnormaler Chromosomensatz ist fast immer mütterlichen Ursprungs, d. h. der Embryo erhält ihn von der Eizelle.
- Je älter die Eizellen sind, desto wahrscheinlicher ist es, dass der Embryo Chromosomenanomalien aufweist, was wiederum normal ist.
- Der Einfluss von Chromosomenfehlern auf die Morphologie des Embryos (wie der Embryo unter dem Mikroskop aussieht) ist am 5.-6. Entwicklungstag unbedeutend. Das bedeutet, dass der Embryo zwar normal aussieht, aber einen abnormalen Chromosomensatz hat [Alfarawati et al., 2011]
Welcher Anteil der Embryonen im Blastozystenstadium wird voraussichtlich einen normalen Chromosomensatz haben?
Diagramm 1. Anteil der Blastozysten mit einem normalen Chromosomensatz bei Frauen verschiedener Altersgruppen nach S. Munne et al.
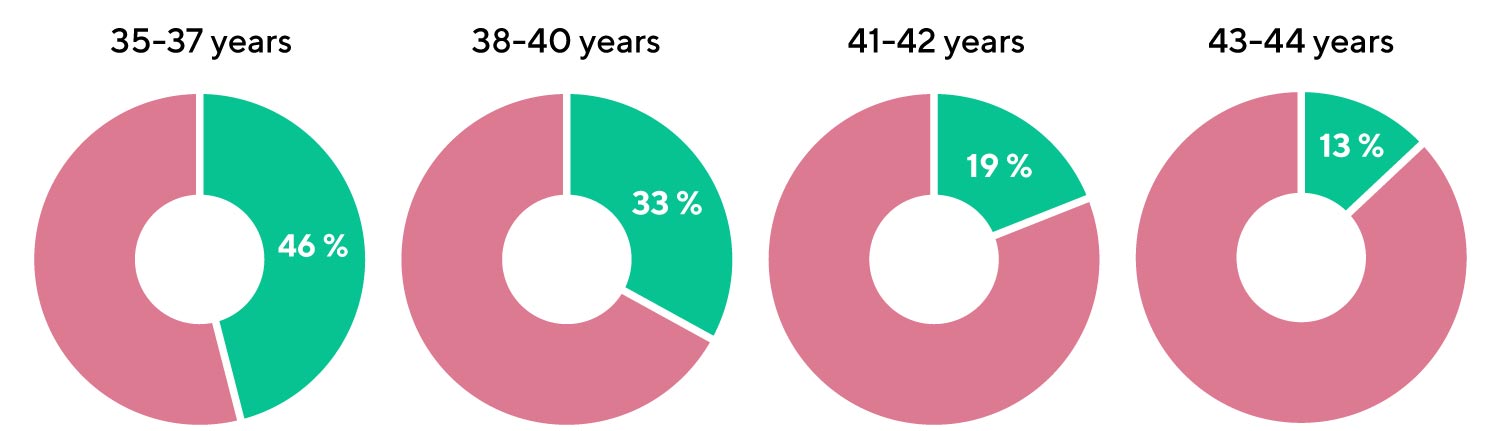
[S. Munne et al. Blastocysts needed to transfer at least one euploid embryo: data from 10,852 pre-implantation genetic screening (PGS) cycles. Fertility Sterility September 2015 Volume 104, Issue 3, Supplement, Pages e13–e14]
- In der Altersgruppe 35-37 wird erwartet, dass jede zweite Blastozyste einen normalen Chromosomensatz aufweist
- Im Alter von 43 Jahren wird voraussichtlich nur noch eine von 8 Blastozysten einen normalen Chromosomensatz haben
Diagramm 2. Anteil der chromosomal normalen Blastozysten in Abhängigkeit vom Alter der Frau. O.L.G.A. Fruchtbarkeitsdaten von 2019 bis 2022.

In den Daten, die wir bei O.L.G.A. Fertility von 2019 bis 2022 erhoben haben, stehen die Anteile chromosomal normaler Blastozysten in Abhängigkeit vom Alter der Frau im Einklang mit einer früheren Studie von S. Munne et al.
I.2. PGT-A-Gentests an menschlichen Embryonen
Kann man feststellen, welche der Blastozysten mit normaler Morphologie ("gut aussehend") einen normalen Chromosomensatz haben und welche nicht?
— Ja! Es gibt diese Möglichkeit, die PGT-A genannt wird.
Was ist PGT-A?
PGT-A steht für Preimplantation Genetic Testing for Aneuploidies (Aneuploidie – ein abnormer Chromosomensatz). Bei dieser genetischen Untersuchung von Embryonen werden die normalen Embryonen unter den verfügbaren Embryonen ausgewählt. Durch den Ausschluss abnormaler Embryonen wird die Lebendgeburtenrate pro übertragenem Embryo erhöht. Dies geschieht, indem die Tests die Embryonen mit abnormalem Chromosomensatz identifizieren, welche zu Einnistungsfehlern und Schwangerschaftsverlusten führen würden, und diese nicht in die Gebärmutterhöhle übertragen werden.
Was ist der Zweck von PGT-A?
PGT-A macht die Embryonen nicht besser. PGT-A wählt Embryonen mit einem normalen Chromosomensatz aus den verfügbaren Embryonen aus, um diese für den Embryotransfer zu verwenden.
Was ist der Zweck von PGT-A?
PGT-A macht die Embryonen nicht besser. PGT-A wählt Embryonen mit einem normalen Chromosomensatz aus den verfügbaren Embryonen aus, um diese für den Embryotransfer zu verwenden.
Wie wird PGT-A durchgeführt?
PGT-A testet den Chromosomensatz in der DNA, die der embryonalen Plazenta entnommen wurde. Embryonen mit einem abnormalen Chromosomensatz führen nicht zu einer gesunden Lebendgeburt und werden daher von der Verwendung ausgeschlossen. Embryonen mit einem normalen Chromosomensatz werden für den Embryotransfer verwendet.
Was sind die Ziele der PGT-A?
- Verringerung der Fehlgeburtenrate
Erhöhung der Lebendgeburtenrate pro Embryotransfer
Verkürzung der Zeit bis zur Geburt eines Kindes (Verringerung der Anzahl der Embryotransfers, bevor ein Kind geboren wird)
Wie lauten die Zahlen?
Schaubild 3. STAR1-Studie im Vergleich zu SART (Nationaler zusammenfassender Bericht USA 2014-2017) Schwangerschaftsresultate

STAR — Rate der anhaltenden Schwangerschaften pro Transfer, wobei zu beachten ist, dass alle anhaltenden Schwangerschaften zu einer Lebendgeburt führten
SART — Lebendgeburtenrate pro Embryotransfer
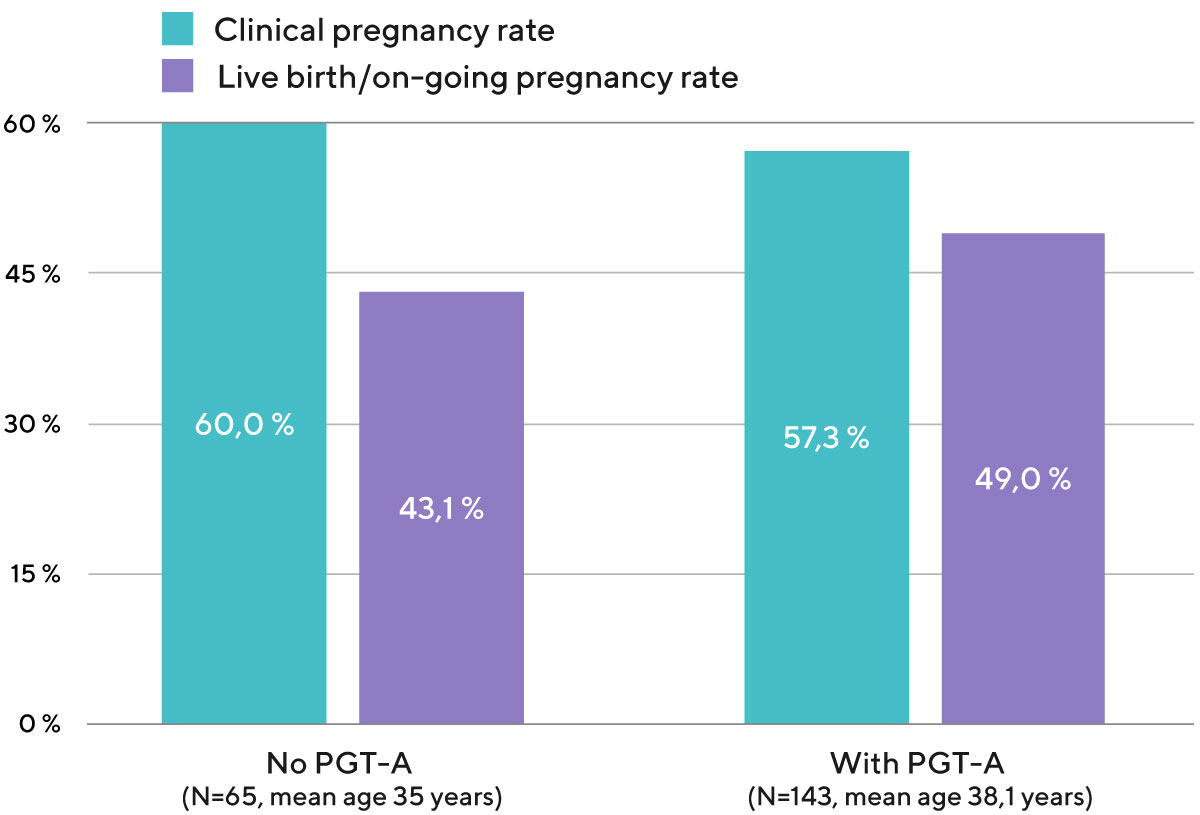
Die Lebendgeburtenrate pro Transfer eines Embryos nach PGT-A liegt bei O.L.G.A. Fertility bei 51%. Das bedeutet, dass in unserer Klinik 51% der Transfers eines einzelnen Embryos mit normalem Chromosomensatz zur Geburt eines Kindes führen (Diagramm 4).
Diagramm 4. Klinische Schwangerschaftsrate und Lebendgeburten-/Schwangerschaftsrate pro Embryotransfer mit eigenen Eizellen, je nachdem, ob PGT-A zur Überprüfung des Chromosomenstatus des Embryos verwendet wurde oder nicht (Daten aus den Embryotransfers, die von 2020 bis 2021 durchgeführt wurden).
Wer kann von der Verwendung von PGT-A zur Steigerung des IVF-Erfolgs profitieren?
II. Mütterliche Ursachen für Schwangerschaftsverlust und IVF-Versagen
Die mütterlichen Ursachen für den Schwangerschaftsverlust und das Scheitern der IVF können hormoneller, entzündlicher oder immunologischer Natur sein. Die Ursachen können mit dem Zustand der Organe des Fortpflanzungssystems oder anderer Organe und Systeme des Körpers zusammenhängen. Oft gibt es bei unseren Patientinnen mehrere Ursachen, warum eine anhaltende Schwangerschaft und eine Lebendgeburt noch nicht erreicht werden konnten.
II.1. Verpassen des Einnistungsfensters – der Hauptgrund für das Scheitern der Einnistung in frischen IVF-Zyklen
Der Vorgang, bei dem sich der Embryo in der Gebärmutter festsetzt, wird als Implantation bezeichnet. Die Einnistung beginnt mit der Erkennung bestimmter Rezeptoren auf der Oberfläche der Gebärmutterschleimhaut durch Rezeptoren auf der Oberfläche des geschlüpften Embryos.
Das Einnistungsfenster ist der Zeitraum, in dem diese Rezeptoren in der Gebärmutterschleimhaut vorhanden sind, in der Regel 5-7 Tage nach dem Beginn der Progesteronproduktion durch das Eibläschen.
Normalerweise beginnt die Progesteronproduktion in einem natürlichen Zyklus mit dem Tag des Eisprungs. Daher sind die Rezeptoren auf den Zellen der Gebärmutterschleimhaut in der Regel 5-7 Tage nach dem Eisprung bereit für die Begegnung mit dem Embryo. Gleichzeitig ist der Embryo, nachdem er den Prozess des Schlüpfens aus der Hülle vollzogen hat, 5-7 Tage nach dem Eisprung bereit für die Einnistung.
Die Natur hat diese beiden Prozesse der embryonalen und endometrialen Bereitschaft zur Einnistung sehr geschickt synchronisiert:
- Der Embryo ist 5-7 Tage nach dem Eisprung bereit für die Einnistung (Bild 3).
- Die Gebärmutterschleimhaut ist 5-7 Tage nach dem Eisprung bereit für die Einnistung (Bild 4).
Abbildung 3. Der Embryo ist 5-7 Tage nach dem Eisprung bereit für die Einnistung

Abbildung 4: Die Gebärmutterschleimhaut ist 5-7 Tage nach dem Eisprung bereit für die Einnistung
 Abbildung 4 veranschaulicht, wie geschickt die Natur die Vorgänge in den Eierstöcken und der Gebärmutter in einem natürlichen Menstruationszyklus synchronisiert.
Abbildung 4 veranschaulicht, wie geschickt die Natur die Vorgänge in den Eierstöcken und der Gebärmutter in einem natürlichen Menstruationszyklus synchronisiert.
FSH stimuliert das Follikelwachstum von Tag 4 bis 14.
Ein Follikel (eine Blase mit einer Eizelle darin) wächst und produziert Östrogen.
Östrogen lässt die Gebärmutterschleimhaut wachsen.
Beim Eisprung wird eine Eizelle freigesetzt und das Zeitfenster für die Einnistung festgelegt.
Normalerweise beginnt die Progesteronproduktion unmittelbar nach dem Eisprung.
Progesteron ist dafür verantwortlich, dass die Gebärmutterschleimhaut für den Embryo aufnahmefähig wird.
Normalerweise wird die Gebärmutterschleimhaut 5-7 Tage nach Beginn der Progesteronproduktion empfänglich für den Embryo.
Der Zeitraum, in dem die Gebärmutterschleimhaut bereit ist, den Embryo zu erkennen und aufzunehmen, wird als Implantationsfenster bezeichnet
Der Zeitpunkt des Beginns der Progesteronproduktion bestimmt das Einnistungsfenster.
Die Stimulation der Eierstöcke kann jedoch zu einer Desynchronisation dieser beiden Prozesse führen: der Bereitschaft zur Einnistung des Embryos und der Bereitschaft der Gebärmutterschleimhaut. Dies geschieht aufgrund der supraphysiologischen Hormonkonzentration im Körper. In vielen stimulierten Zyklen beginnt die Progesteronproduktion zu früh – bereits mehrere Tage vor der Eizellentnahme (was dem Eisprung entspricht).
Wenn die Progesteronproduktion früher als am Tag der Embryonenbildung (Eizellentnahme oder Tag des Eisprungs) einsetzt, sind die Rezeptoren in der Gebärmutterschleimhaut, die den Embryo hätten erkennen können, früher vorhanden. Wenn der Embryo das Stadium des Schlüpfens der Blastozyste erreicht, sind die Rezeptoren in der Gebärmutterschleimhaut nicht mehr vorhanden und der Dialog zwischen Embryo und Gebärmutterschleimhaut ist nicht mehr möglich. Die Einnistung findet nicht statt!
Abbildung 5. Die Desynchronisation der Einnistungsbereitschaft von Embryo und Gebärmutterschleimhaut ist einer der häufigsten Gründe für das Scheitern der Einnistung bei frischen IVF-Zyklen

II.2. Wiederherstellung des Dialogs zwischen dem Embryo und der Gebärmutter, indem Sie in Ihrem IVF-Prozess einen Schritt nach dem anderen machen
Der fehlende Dialog zwischen dem Embryo und der Gebärmutterschleimhaut kann vermieden werden, indem eine Aufgabe nach der anderen erledigt wird.
Der erste Schritt besteht darin, durch eine individuell abgestimmte Stimulation kompetente Eizellen und lebensfähige Embryonen zu erzeugen. Bei dieser Stimulation konzentrieren wir uns ausschließlich auf die Follikel, Eizellen und Embryonen. Es ist noch nicht möglich, sich auch um die Gebärmutterschleimhaut zu kümmern.
Wenn die Blastozysten fertig sind, halten wir die Zeit für sie an, indem wir sie schonend einfrieren. Wenn wir die Zeit für die Embryonen angehalten haben, können wir uns auf die optimale Vorbereitung der Gebärmutter für den Embryotransfer konzentrieren.
Für den Embryotransfer wählen wir einen separaten Zyklus, in dem wir uns auf die Gebärmutterschleimhaut konzentrieren, mit dem Ziel, zum optimalen Zeitpunkt einen Embryo in die optimal vorbereitete Gebärmutterschleimhaut zu übertragen. Normalerweise ist nach dem stimulierten Zyklus ein Menstruationszyklus erforderlich, damit die Eierstöcke keine Restmengen an Progesteron mehr produzieren. Daher empfehlen wir eine Pause von einem Zyklus zwischen der Eizellentnahme und dem Embryotransfer.
Diagramm 5. Kumulative Lebendgeburtenrate in allen Gruppen von Patienten, die einen Embryotransfer erhielten, innerhalb von 1131 aufeinanderfolgenden Embryotransfers bei O.L.G.A. Fertility von 2019 bis 2021)
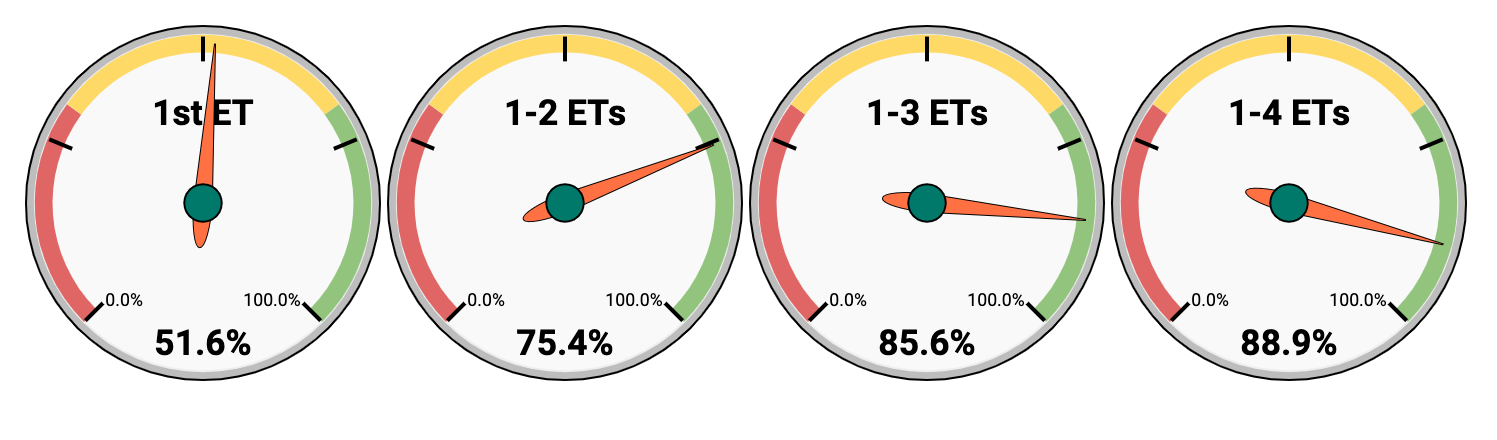
Bei O.L.G.A. Fertility haben Sie:
- 51.6% Chance auf eine Lebendgeburt nach 1 ET (Embryotransfer)
- 75.4% Chance auf eine Lebendgeburt nach 2 ETs
- 85.6% Chance auf eine Lebendgeburt nach 3 ETs
- 88.9% Chance auf eine Lebendgeburt nach 4 ETs
Wenn wir also beharrlich und konsequent auf das Ziel hinarbeiten, liegt die Chance, nach 4 Embryotransfers bei O.L.G.A. Fertility ein Baby zu bekommen, bei 88,9%.
Watch our Webinars
Because of multiple reasons of miscarriages and IVF failures we split IVF process in parts to solve each of them and achieve live birth

By Dr. Olga Zaytseff
The founder of O.L.G.A. Clinic
How to identify challenges, grow competent eggs, create viable embryos and screen them

By Dr. Olga Zaytseff
The founder of O.L.G.A. Clinic
This webinar about optimizing uterus by hysteroscopy, boosting uterine lining by specific medication, precise timing of embryo transfer with the help of ERA test, hormonal and immune treatment

By Dr. Elena Lapina
Head doctor and co-founder of O.L.G.A. Clinic
How to identify and solve them to achieve successful pregnancy and live birth

By Dr. Elena Lapina
Head doctor and co-founder of O.L.G.A. Clinic
Hot and controversial topics explained from the very beginning — basic genetics, indications, embryo biopsy and freezing, challenges, results and new frontiers

By Dr. Anna Gusareva
Embryo Lab Chief at O.L.G.A. Clinic
How embryos are created and grow in the lab? How embryologists make sure that embryos feel at home in the lab? How to choose the best embryo that will result in live birth?

By Dr. Anna Gusareva
Embryo Lab Chief at O.L.G.A. Clinic
How to make decision and process comfortable and friendly for you, and your result — efficient.

By Dr. Olga Zaytseff
The founder of O.L.G.A. Clinic
Valeria shares different aspects of her work and show even examples of excellent egg donor choices based on physical characteristics and non-physical parameters, such as education, personal motivation, occupation...

By Valeria Sergeeva
The leading egg donation expert at O.L.G.A. Clinic
Egg donation… Embryo adoption…
How normal is the whole process? Who are the donors and what I should/can know about them? Where is the border of my influence?

By Valeria Sergeeva
The leading egg donation expert at O.L.G.A. Clinic
We prepared a very special video where egg donors personally tell about themselves, their principles of life, their reasons to donate and the philosophy of this huge project called "Egg Donation" at O.L.G.A Fertility Clinic

By Valeria Sergeeva
The leading egg donation expert at O.L.G.A. Clinic


By Tatiana Varzaeva
Perinatal psychologist at O.L.G.A. Clinic